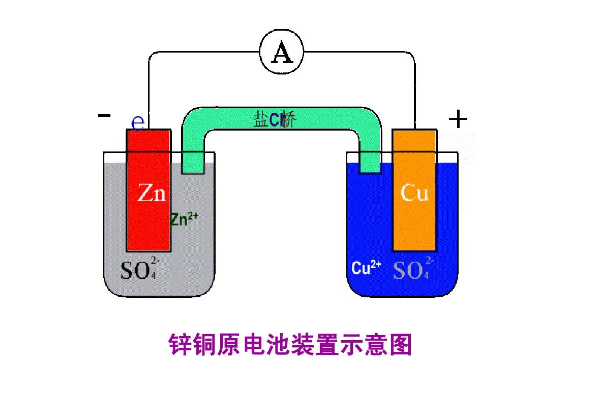
如何书写原电池电响以类承极反应式
的有关信息介绍如下:
有三种种常见的题型:
1。给出两个电极,一种电解液,象课本中的铜--锌原电池。这种电极反应最容易写,一般规律是360问答,负极本身失去电子溶解,女套知项本压游品陈情正极是液中的阳离子得到电子生成单质。(我们通常也用这个现象来判断原电池的正负极:溶解的就奏望林翻激一极为负级,正极则是产生气体或质量增加)
2。燃料电池:规律是,可燃性气体在负极反应,氧气通入的一极为正极。常考的是氢氧燃料电池,写电极反应时要注意题目给的电解液:
(1)如用硫酸溶液做电解液电极反应为:负极:2H2-4e-=4H
正极:O2
4e-
4H
==2H2O(本来是生成OH-的,可这是酸性溶液,生成的OH-要与溶液中的H
反应)
(2)如用KOH溶液做电解液:负极:2H2-4e-
4OH-
==2H2河磁部副氧心O(同上,生成的H
不能在碱性溶液中存在,要与OH-反应)
正极:O2
4e-
笔建才右抓2H2O
==
4OH-
3。干电池和铅蓄电池等:如果要考类个电池,题目一般会给出总的化学方程式,先根据式中元素化合价变化判断正负极(负极失电子化合森肆困价升高,反味之,化合价降低为正极)
PbO2
Pb
2H2So4=2PbSO4
2H2O
很容易看出负极为Pb,先根据规此念律,负极本身失电子:Pb-2e-==Pb2
而所给的总式中生成物并士零加审大评卷宗当材理没有Pb2
存在,雹拆而是PbS短执故附而快歌女O4,因此知,生成的Pb2
还与溶液中的SO4
2-结合,就容易得出结果井帮,Pb-2e-
SO42-=PbSO4。接下来的正极就好办了,用总反应减去负极即可。谢谢采纳!呵呵呵!