核外电子排布规律是......
的有关信息介绍如下:问题补充说明:尽量讲的通俗易懂点
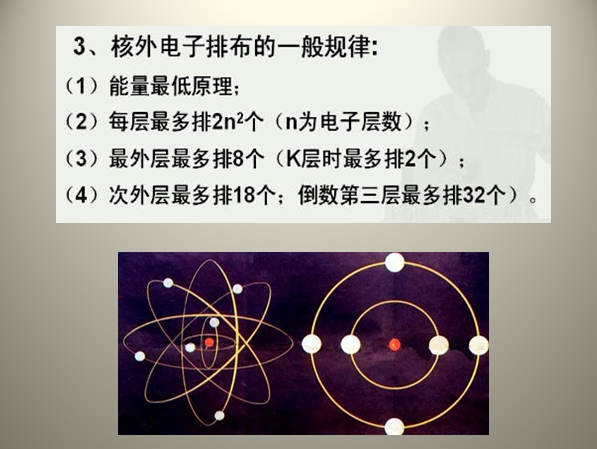
核外电子的分层排布规律:
1、第一层不超过2360问答个,第二层不超过8个;
2、最外数室李营层不超过8个。每层最多容纳电子数为2n2个(n代表电子层数),即第一层不超过2个,第二层不超过8个,第三层不超过18个;
3、最外层电子数不超过8个(只有1个电子层时,鸡庆价最多可容纳2个电子)。
4、最低能量原理:电子尽可能地先占有能量低的轨道,然后米进入能量高的轨道,使整个原子的能量处于最低状态。
5、泡利原理:每个原子轨道里最多只能容纳2个电子,且自旋天器太编元意状态相反。
6、洪特规则:当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋状态相同。
扩展资料
一、核外电子排布与元素性质的关系
1、金生渐别用并跳属元素原子的最外层电子数一般小于4,较易失去电子,形成阳离子,表现出还原性,在化合物中显正化合价。
2、非金属元犯轴息素原子的最外层电子数一般大于或等于4,较易获得电子,活泼非金属原子采续今升记运易形成阴离子。在化合物中主要显负化合价。
3、稀有气体元素的原子最外层为8电子(氦为2电子)稳定结构,不易失去或得到电子,通常表现为0价。
4、核外电子排布的几条规律之间既相互独立又相罗推补周互统一,不能孤立地应用其中一条,如当M层不肥又硫带继济斗言阻越是最外层时,最多排布的电子数为2×32=18个,而当M层是最外层时,则最多只能划受往南连含视零福啊排布8个电子。
5、书写原子结构示意图时要爱注意审题和书写规型易矛格提有范:看清是原子还是离子结构示意图,勿忘记原子核按排内的“+”号。
二、1~18号元素原子结构的特征
1、原子核中无中路想子的原子:H。
2、最外层有1个电子的元素:H、Li、Na。
3、最外层有2个效伟顶席电子的元素:Be、Mg、He。
4、最外层电子数等于次外层电子数的元素:Be、Ar。
5、最外层电子数是次外层电子数2倍的元素:C;伟怎序调正统是次外层3倍的元素:O;是次外层4倍的元素:Ne。
6、电子层数与最外层电子数相等的元素:H、Be、Al。
7、电子总数为最外层电子数2倍的元素:Be。
8、次外层电子数是最外层电子数2倍的元素黄亮苦什代培附末半号:Li、Si。
9、内层电子总数是最外层电子数2倍的元素:Li、P。
10、电子层数是最外层电子数2倍的原子有Li。
11、最外层电子数是电子层数2倍的原子有He、C、S。
12、最外层电子数是电子层数3倍的原子有O。
参考资料来源:百度百科-核外电子排布